Il est désormais possible d’envisager que des patients atteints de diabète de type 2 nécessitant une insulinothérapie puissent recevoir une seule injection par semaine, sous la forme d’une insuline basale hebdomadaire. En effet, deux essais cliniques, publiés fin juin 2023 dans le New England Journal of Medicine et le JAMA, deux revues médicales américaines, montrent qu’une nouvelle insuline en prise hebdomadaire permet de parvenir à un contrôle glycémique significativement meilleur que celui obtenu avec une insuline administrée chaque jour. L’insuline hebdomadaire administrée dans ces deux essais cliniques porte le nom d’insuline icodec (laboratoire Novo Nordisk).
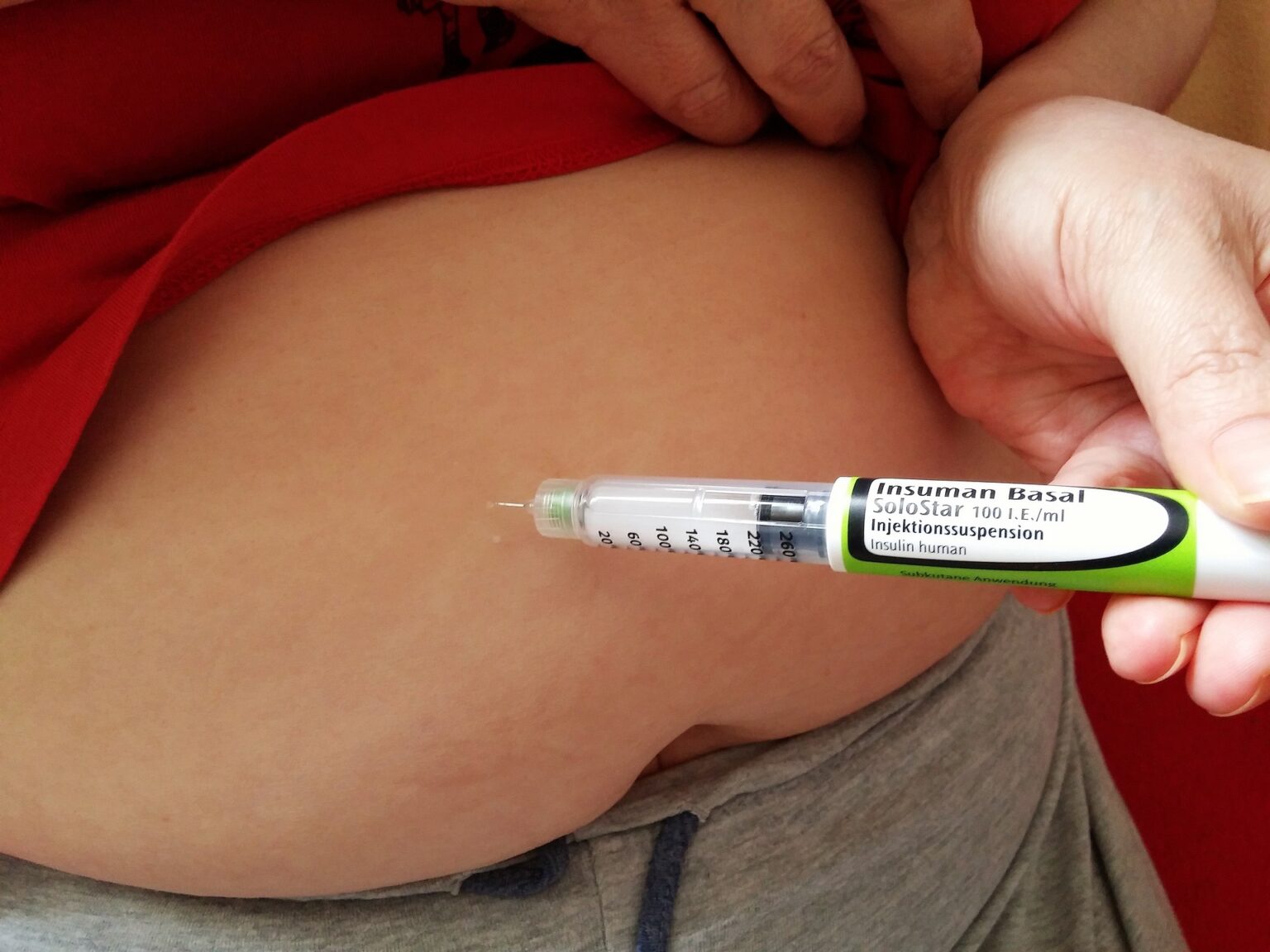
Chez les patients vivant avec un diabète de type 2 (DT2), l’évolution progressive de la maladie diabétique peut conduire à la mise en route d’un traitement insulinique lorsque la sécrétion d’insuline par l’organisme devient insuffisante. Il est alors nécessaire pour ces patients DT2 de s’injecter une insuline basale, destinée à couvrir les besoins de fond en insuline. C’est donc le plus souvent par une insulinothérapie basale isolée que l’on débute, même si l’évolution de la maladie diabétique peut nécessiter par la suite une intensification du traitement. Dans ce cas, celui-ci correspond à ce que l’on appelle un schéma basal-bolus, qui associe une insuline basale (insuline lente) et une insuline apportée par un bolus, en l’occurrence une injection d’insuline rapide au moment des repas.
Pouvoir disposer d’une insuline basale hebdomadaire diminuerait donc les contraintes liées aux injections quotidiennes et devrait pouvoir améliorer l’adhésion au traitement et son observance. Un traitement par l’insuline icodec pourrait ainsi réduire le délai avant la mise en route d’un traitement insulinique et diminuer le nombre d’injections annuelles d’au moins 365 à seulement 52.
L’insuline icodec présente des caractéristiques structurelles particulières
La structure de l’insuline icodec diffère de celle des analogues d’insuline déjà commercialisés. Une chaîne carbonée a été insérée. Cela permet à cette insuline de pouvoir se fixer sur l’albumine plasmatique une fois qu’elle passe dans la circulation sanguine, et ainsi d’augmenter sa durée d’action. L’insuline icodec comporte par ailleurs des modifications au niveau de trois acides aminés qui ont été remplacés par d’autres. Ceci entraîne une prolongation supplémentaire de l’activité de la molécule. En effet, ces substitutions d’acides aminés se situent à des emplacements jouant un rôle majeur à la fois dans la fixation de l’insuline sur son récepteur cellulaire puis sur sa libération de son récepteur.
L’ensemble de ces modifications structurelles aboutit à ralentir la vitesse à laquelle cette insuline se lie et se détache de son récepteur, avec pour conséquence que la demi-vie de l’insuline icodec est de l’ordre de 196 heures (soit un peu plus d’une semaine). Le résultat est un effet hypoglycémiant étalé sur une période de 7 jours. D’où la possibilité de l’utiliser à raison d’une injection hebdomadaire.
L’essai clinique randomisé de phase 3, publié dans le New England Journal of Medicine le 24 juin 2023, a inclus 492 patients adultes diabétiques de type 2 non antérieurement traités par insuline. Il a été conduit dans 143 centres répartis dans 12 pays. La moitié des participants a reçu l’insuline hebdomadaire icodec, l’autre moitié recevant une injection quotidienne de glargine U100. Celle-ci a été sélectionnée comme comparateur dans la mesure où il s’agit de l’insuline basale quotidienne la plus couramment utilisée.
Le critère principal de jugement de cet essai, baptisé ONWARDS 1, était la diminution, entre le début de l’étude et la 52e semaine, du taux de l’hémoglobine glyquée (HbA1c). Ce marqueur biologique est le reflet de la glycémie sur une durée de trois mois. Il est pour ainsi dire la mémoire du contrôle glycémique. On considère qu’un diabète est équilibré si le taux d’hémoglobine glyquée est compris entre 6 et 7 %, selon les âges.
A la 52e semaine, une baisse plus importante du taux d’hémoglobine glyquée (HbA1c) a été observée dans le groupe traité par l’insuline icodec par rapport à celui recevant l’insuline glargine U100. Le taux d’HbA1c est passé de 8,50 % à 6,93 % dans le groupe icodec et de 8,44 % à 7,12 % dans le groupe glargine U100. Ce résultat montre que l’insuline icodec fait donc tout aussi bien, sinon mieux, que l’insuline glargine U100 en termes de réduction de l’hémoglobine glyquée. Les spécialistes parlent de la non-infériorité et de la supériorité de l’insuline icodec.
Les investigateurs de l’essai clinique ont également évalué le temps passé dans la cible (TIR, time in range, en anglais), à savoir le pourcentage de temps passé par une personne diabétique dans la plage glycémique cible entre la 48e et la 52e semaine, en l’occurrence le temps où la glycémie était comprise entre 0,70 et 1,8 g/L. Entre la 48e et la 52e semaine, les participants ayant reçu l’insuline icodec ont passé plus de temps dans la plage glycémique cible que ceux recevant la glargine U100 (71,9 % vs. 66,9 %). L’essai a été prolongé jusqu’à la semaine 78. Entre la 74e et la 78e semaine, cette différence s’est maintenue (70,2 % avec icodec vs. 64,8 % avec glargine U100), ce qui correspond à environ 64 minutes de temps supplémentaire passé dans la cible par jour avec l’insuline icodec.
À la semaine 52, un plus grand nombre de participants du groupe insuline icodec avait atteint un taux d’hémoglobine glyquée inférieur à 7 % (57,6 % vs. 45,4 % dans le groupe glargine U100) sans présenter d’épisodes hypoglycémiques significatifs sur le plan clinique ou d’hypoglycémie sévère. Cette réduction de l’hémoglobine glyquée avec l’insuline icodec s’est maintenue jusqu’à la semaine 78 (fin de l’essai).
La sécurité d’emploi de l’insuline icodec a également été évaluée. Il ressort que le nombre d’épisodes hypoglycémiques cliniquement significatifs était comparable dans les deux groupes (12.4 % pour l’insuline icodec, 13.4% pour la glargine U100).
L’efficacité et la sécurité d’emploi de l’insuline hebdomdaire icodec ont été et font actuellement l’objet d’autres essais cliniques. Au total, six essais l’évaluent. Trois essais concernent des patients diabétiques de type 2 non antérieurement traités par l’insuline. Il s’agit de l’essai ONWARDS 1 (dont il vient d’être question), de ONWARDS 3 (essai randomisé en double aveugle, conduit sur 26 semaines) et de ONWARDS 5 (essai randomisé en double aveugle sur 52 semaines, avec comparaison de l’insuline icodec à d’autres analogues d’insuline, dont la glargine U300 et l’insuline dégludec). Les essais ONWARDS 2 et 4 concernent des patients DT2 ayant déjà été traités par insuline. Enfin, ONWARDS 6 a inclus des patients diabétiques de type 1.
Les résultats de l’essai ONWARDS 3 ont été publiés dans le JAMA le 24 juin 2023. Cet essai randomisé multicentrique (92 sites dans 11 pays) a évalué l’efficacité et la sécurité de l’insuline hebdomadaire icodec comparativement à l’insuline quotidienne dégludec chez des adultes diabétiques de type 2 n’ayant jamais été traités par de l’insuline. Au total, 588 patients ont été inclus (294 dans chaque groupe) dans cet essai qui comprenait une durée de traitement de 26 semaines et un suivi de 5 semaines.
Le principal critère de jugement était le changement du taux de l’hémoglobine glyquée entre le début de l’étude et la semaine 26. Les investigateurs ont également évalué le nombre d’épisodes hypoglycémiques de niveau 2 (cliniquement significatifs, glycémie inférieure à 0,54 g/L) ou de niveau 3 (hypoglycémie sévère, associée à un trouble cognitif sévère nécessitant une prise en charge).
Le taux moyen d’HbA1c est passé de 8,6 % à 7,0 % à la 26e semaine dans le groupe icodec et de 8,5 % à 7,2 % dans le groupe dégludec. L’insuline icodec a ainsi entraîné une baisse plus importante que l’insuline dégludec après 26 semaines de traitement, confirmant à la fois la non-infériorité et la supériorité de l’insuline hebdomadaire chez des patients DT2 non antérieurement traités par insuline. Cette diminution de l’HbA1c de 0,2 % après 26 semaines de traitement est cependant marginale sur le plan clinique.
Par ailleurs, durant la durée de l’essai, le taux combiné des hypoglycémies de niveau 2 et 3 a été significativement plus élevé dans le groupe icodec que dans le groupe dégludec, mais faible dans les deux groupes. Dans cet essai ONWARDS 3, le comparateur était l’insuline dégludec qui présente un moindre risque d’hypoglycémie que l’insuline glargine U100 (évaluée dans l’essai ONWARDS 1).
En mai 2023, les résultats d’ONWARD 3 ont été publiés dans la revue The Lancet Diabetes & Endocrinology. D’une durée de 26 semaines, cet essai de phase 3 a comparé l’efficacité et la sécurité d’emploi de l’administration de l’insuline icodec à l’insuline quotidienne dégludec chez des patients DT2 qui étaient faiblement contrôlés avec une ou deux injections d’insuline basale quotidienne. L’injection hebdomadaire d’icodec a été associée à un meilleur contrôle glycémique sans augmentation significative du risque d’hypoglycémie. Le nombre d’hypoglycémies dans le groupe icodec était néanmoins numériquement supérieur, ce qui pourrait poser problème chez des personnes âgées qui n’ont pas souvent conscience qu’elles sont en hypoglycémie.
Les résultats d’ONWARDS 4 sont également parus dans The Lancet Diabetes & Endocrinology en mai 2023. Cet essai multicentrique concerne des patients DT2 dont l’évolution progressive de la maladie diabétique nécessite un schéma basal-bolus. Dans cet essai, les participants du groupe icodec prenaient donc une insuline hebdomadaire et une insuline post-prandiale (après le repas). Chaque groupe traité comprenait 291 patients.
Cet essai a comparé, sur une durée de 26 semaines, l’insuline hebdomadaire icodec à l’insuline quotidienne glargine U100. Il a été montré que ces deux traitements ont une efficacité comparable en termes de réduction de l’hémoglobine glyquée. Le temps dans la cible (70-1,8 g/L) était comparable dans les deux groupes (66,9 % dans le groupe icodec, 66,4 % dans le groupe glargine).
L’incidence combinée des hypoglycémies de niveau 2 et 3 était similaire dans les deux groupes traités. Cela dit, dans la mesure où cet essai avait exclu les patients les plus à risque d’hypoglycémie (en l’occurrence ceux qui avaient déjà présenté une hypoglycémie sans le savoir et ceux qui avaient fait une hypoglycémie sévère au cours de l’année passée), des études supplémentaires sont nécessaires pour préciser ce point.
Aux États-Unis, Novo Nordisk a déposé une demande d’autorisation de mise sur le marché pour l’insuline icodec auprès de la Food and Drug Administration (FDA). Une décision de l’agence américaine du médicament est attendue en avril 2024. Selon le laboratoire, des demandes similaires ont été soumises au Canada, en Europe, en Australie, en Suisse et au Brésil.
BIF : une insuline liée à une immunoglobuline
L’insuline icodec n’est pas la seule insuline hebdomadaire en développement clinique. Des études de phase 3 sont également en cours avec l’insuline efsitora alfa (également dénommée BIF, pour basal insulin Fc). Développée par la firme firme Eli Lilly, cette insuline basale est une protéine obtenue en greffant une immunoglobuline sur une chaîne d’une molécule d’insuline*. Ce procédé permet d’obtenir une insuline ayant une longue durée de vie, de l’ordre de 17 jours et dotée d’une activité hypoglycémiante d’une durée d’au moins 5 jours.
S’agissant d’insulines basales hebdomadaires, il importe de disposer d’une molécule ayant un profil pharmacocinétique quasiment plat (near-flat action profile), qui se traduit par de faibles fluctuations de la glycémie au sein de la journée et d’un jour à l’autre. C’est à cette condition que l’on peut éviter le risque hypoglycémique comme la survenue d’hyperglycémies. En d’autres termes, le profil d’activité d’une telle insuline doit être très différent entre les pics et les creux.
Des études ont montré que l’insuline BIF, qui a une demi-vie de 17 jours, a un faible rapport pic-creux (peak-to-trough ratio), qui se traduit par une variation inférieure à 15 % dans la concentration en insuline. Ce faible ratio pic-creux devrait, en principe, permettre d’obtenir des taux de glucose sanguins intra- et inter-journaliers plus stables.
Un essai multicentrique randomisé de phase 2 a été mené dans 44 centres aux États-Unis, Porto Rico et au Mexique. Publié en mars 2023 dans The Lancet Diabetes and Endocrinology, il a conclu à une efficacité et une sécurité d’emploi comparable de l’insuline hebdomadaire BIF et de l’insuline quotidienne dégludec chez des patients ayant un diabète de type 2 déjà traités par insuline. Les taux de glycémie à jeun étaient cependant plus élevés avec BIF qu’avec dégludec.
Les données recueillies lors de cet essai seront utilisées pour développer un algorithme permettant de calculer au mieux les doses qui seront administrées dans les essais de phase 3 qui seront prochainement conduits auprès de patients diabétiques déjà traités par insuline ou non insulinés jusqu’à présent.
Publié dans la revue Diabetes Care, un essai clinique multicentrique randomisé de phase 2 a évalué sur 26 semaines, avec 5 semaines de suivi, l’efficacité et la sécurité de l’insuline hebdomadaire BIF cette fois chez des patients adultes diabétiques de type 2 non antérieurement traités par l’insuline. Cette étude, comparant l’insuline hebdomadaire BIF (129 patients) à l’insuline quotidienne dégludec (135 patients), a été menée dans 61 centres en Argentine, Allemagne, Pologne et aux États-Unis.
Il ressort que l’insuline BIF a permis d’obtenir un contrôle glycémique comparable à celui de l’insuline quotidienne dégludec. L’insuline BIF a fait aussi bien que le dégludec en termes de réduction de l’hémoglobine glyquée (HbA1c), la baisse de l’HbA1c entre le début de l’étude et la semaine 26 étant de – 1,2 % pour BIF et de -1,26 % pour dégludec. De même, à la semaine 26, la proportion de patients dont l’HbA1c était descendue sous les 7 % a été comparable dans les deux groupes (62,3 % avec BIF vs. 68,6 % avec dégludec).
Le temps passé dans la cible glycémique était comparable pour les deux préparations insuliniques (supérieur ou égal à 75 % sur une période de 24 heures d’ici la fin du traitement). De plus, avec cette insuline basale Fc, l’incidence des hypoglycémies de niveau 1 (< 0,7 g/L ou 3,9 mmol/L) a été similaire dans les deux groupes de traitement. Aucune hypoglycémie sévère (de niveau 3) n’est survenue.
Faciliter l’insulinothérapie basale dans le DT2, voire dans le DT1
L’ensemble de données provenant de ces études de phase 2 et 3 concernant ces deux insulines hebdomadaires permet de penser que ces nouvelles préparations insuliniques devraient transformer le traitement du diabète de type 2 (DT2), et même peut-être celui de certains patients vivant avec un diabète de type 1.
Une étude de phase 2, multicentrique, randomisée, a évalué sur 26 semaines la sécurité d’emploi et l’efficacité de l’insuline basale Fc (BIF) chez 240 patients diabétiques de type 1 (DT1) en comparaison à l’insuline quotidienne dégludec administrée. Au total, 124 ont été traités par BIF, 126 autres ont reçu le dégludec. Durant la durée de l’étude, ces patients DT1 ont continué à prendre leur insuline rapide (destinée à contrôler la glycémie au moment des repas).
Publiés le 1er mai 2023 dans Diabetes Care, les résultats de cet essai multicentrique, conduit dans 49 sites en Espagne, Autriche, Allemagne, Porto Rico, et aux États-Unis, montrent que BIF a une efficacité quasi-identique à celle de l’insuline dégludec en termes de contrôle glycémique. Une différence de 0,17 % a été observée en faveur du dégludec pour ce qui concerne le taux d’hémoglobine glyquée. Elle se situe dans la marge prédite pour conclure à une non-infériorité de BIF par rapport au dégludec.
De plus, le pourcentage de temps dans la cible a été similaire à la 26e semaine dans les deux groupes traités. Les valeurs de la glycémie à jeun étaient cependant significativement plus élevées chez les patients recevant BIF que chez ceux traités par l’insuline dégludec. Aucune différence sur l’incidence des hypoglycémies de niveau 1 et 2 n’a été observée entre les deux traitements.
Éviter l’inertie thérapeutique chez de nombreux patients diabétiques de type 2
En évitant les contraintes des injections quotidiennes, une insulinothérapie basale hebdomadaire pourrait éviter l’inertie thérapeutique de nombreux patients DT2, et donc de lever leurs réticences afin de les encourager à débuter à temps un traitement insulinique.
Dans une même démarche de simplification du traitement, la mise à disposition d’insulines hebdomadaires pourrait inciter à développer des préparations combinant une forme également hebdomadaire d’un agoniste du GLP-1 (glucagon-like peptide-1), autre médicament antidiabétique. En effet, des études ont déjà montré que, par rapport à une prise quotidienne, un traitement hebdomadaire par un agoniste du GLP-1 améliore la glycémie et l’adhésion thérapeutique.
Il est rétrospectivement apparu que BIF était initialement sous-dosé, de l’ordre de 30 % dans cet essai de phase 2. Les données de pharmacocinétiques (concernant l’absorption, la distribution, le métabolisme et l’excrétion de l’insuline BIF) et pharmacodynamiques (effets de cette nouvelle insuline sur l’organisme) recueillies permettront d’améliorer l’algorithme utilisé pour calculer les doses à administrer dans le cadre des prochains essais de phase 3.
Il n’en reste pas moins que, chez le patient diabétique de type 1, la transition d’une insuline basale quotidienne à une insulinothérapie basale hebdomadaire représentera un défi du fait d’une variabilité glycémique au quotidien plus importante que chez les patients DT2. Les insulines hebdomadaires pourraient donc ne pas convenir à la plupart des diabétiques DT1.
Évolution ou révolution dans l’insulinothérapie
On le voit, plus de 100 ans après la découverte de l’insuline, l’insulinothérapie est l’objet de progrès constants (insulines rapides, ultrarapides, ultralentes). Nul ne sait aujourd’hui si les perspectives cliniques offertes par les insulines hebdomadaires correspondront à une évolution, ou à une révolution, dans le traitement du diabète. Mais une chose est sûre : la mise à disposition de ces nouvelles préparations insuliniques représentera une avancée qui modifiera beaucoup les pratiques actuelles, tant pour les patients que pour les médecins prescripteurs, qui devront apprendre à utiliser des nouvelles stratégies de dosage très différentes de celles utilisées actuellement.
Ces nouvelles insulines à très longue durée d’action pourraient donc bien ouvrir une nouvelle ère de l’insulinothérapie. Les prochaines études devraient permettre de mieux définir la place que pourraient occuper ces nouvelles préparations insuliniques dans le traitement du diabète.
Reste à espérer que le coût de ces insulines hebdomadaires sera abordable pour tous les diabétiques, qu’ils résident dans des pays à faibles revenus ou dans des pays riches, comme les États-Unis où le prix des analogues insuliniques reste prohibitif. Ceci est un autre défi.
Marc Gozlan (Suivez-moi sur Twitter, Facebook, LinkedIn, Mastodon)
* L’insuline basale Fc (BIF), également appelée insuline efsitora alfa, est une protéine de fusion qui consiste en un nouveau variant insuline simple chaîne et un domaine Fc d’une immunoglobine IgG2.